[FONT="]Bu ders notumuzda Kimya dersinin Atom ve Yapısı konusu altında; Atom Nedir? Atomun Yapısı ve Özellikleri, Atom Numarası, İyon, İzotop, Allotrop, Elektronların Dizilişi, Elektronik Konfigürasyon vb. başlıklar hakkında detaylı bilgileri bulabilirsiniz.[/FONT]
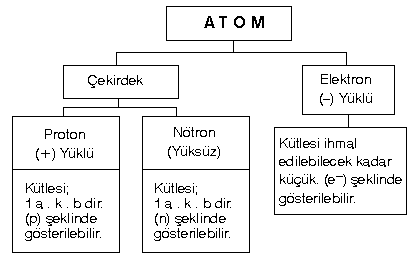
[h=1]ATOM ve YAPISI[/h][FONT="]Elementin özelliğini taşıyan en küçük parçasına denir.[/FONT]
[FONT="]
 [/FONT]
[/FONT]
[h=3]Atom Numarası[/h][FONT="]Bir elementin unda bulunan proton sayısıdır. Protonlar (+) yüklü olduklarından pozitif yük sayısı ya da çekirdek yükü şeklinde ifade edilebilir.[/FONT]
[FONT="]eşitliği yazılabilir.[/FONT]
[FONT="]Nötr (yüksüz) bir için, çekirdekte kaç proton varsa çekirdeğin etrafındaki yörüngelerde de o kadar elektron dolaşır.[/FONT]
[h=3]İYON[/h][FONT="](+) veya (–) yüklü ya da gruplarına iyon denir.[/FONT]
[FONT="]
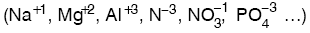 [/FONT]
[/FONT]
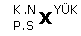 gösterilir.[/FONT]
gösterilir.[/FONT]
[FONT="]Buradan nötron sayısı, elektron sayısı bulunabilir.[/FONT]
[h=3]İZOTOP[/h][FONT="]numaraları aynı kütle numaraları farklı olan atomlara izotop atomlar denir.[/FONT]
[FONT="]
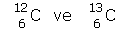 birbirinin izotopudur.[/FONT]
birbirinin izotopudur.[/FONT]
[FONT="]Elmas, grafit, amorf karbon, üç madde de yapısında yalnızca karbon (C) u içerir. Fakat uzaydaki dizilişleri ve bağların sağlamlığı farklı olan maddelerdir.[/FONT]
[FONT="]O2 gazı ve O3 (Ozon) gazı birbirlerinin allotropudur. Allotrop için bilinmesi gereken en önemli özellik ise;[/FONT]
[FONT="]Allotrop maddeler bir başka madde ile reaksiyona girdiklerinde aynı cins ürünler oluşur.[/FONT]
[FONT="]2Ca + O2 ® 2CaO[/FONT]
[FONT="]3Ca + 2/3 O3 ® 2CaO gibi.[/FONT]
[FONT="]Modern Teorisi[/FONT]
[FONT="]1. yörünge : 2.12 = 2 elektron[/FONT]
[FONT="]2. yörünge : 2.22 = 8 elektron[/FONT]
[FONT="]3. yörünge : 2.32 = 18 elektron[/FONT]
[FONT="]4. yörünge : 2.42 = 32 elektron alır.[/FONT]
[FONT="]
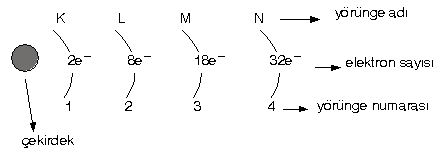 [/FONT]
[/FONT]
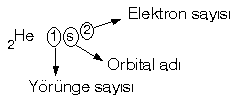
[h=3]Elektronik Konfigürasyon[/h][FONT="]Bir atomun elektronlarının hangi yörüngede olduğu ve orbitallerinin cinsinin belirtildiği yazma düzenine Elektronik konfigürasyon denir.[/FONT]
[FONT="]n : Baş kuant sayısı olup 1, 2, 3, … gibi tam sayılardır. Elektronun hangi yörüngede olduğunu belirtir.
[/FONT]
[FONT="]l : Yan kuant sayısı olup, orbital adı olarak bilinir, s, p, d, f gibi harflerle anılır.[/FONT]
[FONT="]Elektronlar önce düşük potansiyel enerjili orbitallere yerleşirler. Dört değişik enerji düzeyi vardır.[/FONT]
[FONT="]s : Enerji seviyesi en düşük orbitaldir. 2 elektron alabilir.[/FONT]
[FONT="]p : s orbitalinden sonra elektronlar p orbitallerine yerleşir. px , py , pz olmak üzere 3 tanedir. p orbitalleri toplam 6 elektron alabilir.[/FONT]
[FONT="]d : 10 elektron alır ve toplam 5 tanedir. p orbitallerinden sonra elektronlar d orbitallerine yerleşirler.[/FONT]
[FONT="]f : f orbitalleri toplam 14 elektron alır ve 7 tanedir. Enerji düzeyi en yüksek olan orbitaldır.[/FONT]
[FONT="]
 [/FONT]
[/FONT]
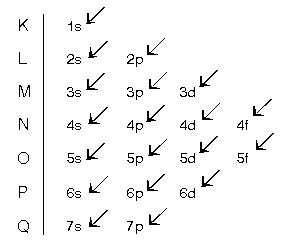
[FONT="]Bir atomun elektronları yörüngelere yerleştirilirken okların sırası takip edilir. Bunlar bu sıra ile yazılırsa aşağıdaki gibi olur.[/FONT]
[FONT="]1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6[/FONT]
[FONT="]
 [/FONT]
[/FONT]
[FONT="]Periyot : Dizilişi yapılan elementin en son yazılan s orbitalinin başındaki sayıya periyot denir.[/FONT]
[FONT="]Grup : Son yörünge orbitalleri s ve p ile bitiyorsa A grubu, d ve f ile bitiyorsa B grubu elementidir.[/FONT]
[h=1]ATOM ve YAPISI[/h][FONT="]Elementin özelliğini taşıyan en küçük parçasına denir.[/FONT]
[FONT="]

[h=3]Atom Numarası[/h][FONT="]Bir elementin unda bulunan proton sayısıdır. Protonlar (+) yüklü olduklarından pozitif yük sayısı ya da çekirdek yükü şeklinde ifade edilebilir.[/FONT]
| Atom numarası = Proton sayısı = Çekirdek yükü |
| Kütle Numarası = Proton sayısı + Nötron sayısı |
[FONT="]Nötr (yüksüz) bir için, çekirdekte kaç proton varsa çekirdeğin etrafındaki yörüngelerde de o kadar elektron dolaşır.[/FONT]
[h=3]İYON[/h][FONT="](+) veya (–) yüklü ya da gruplarına iyon denir.[/FONT]
[FONT="]
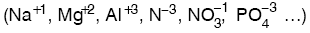
- elektron verirse (+) yüklü iyon oluşur ve katyon olarak isimlendirilir.
- elektron alırsa (–) yüklü iyon oluşur ve anyon olarak isimlendirilir.
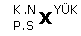
[FONT="]Buradan nötron sayısı, elektron sayısı bulunabilir.[/FONT]
[h=3]İZOTOP[/h][FONT="]numaraları aynı kütle numaraları farklı olan atomlara izotop atomlar denir.[/FONT]
[FONT="]
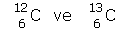
- İzotop atomların kimyasal özellikleri aynıdır. Fiziksel özellikleri farklıdır.
- İzotop iyonların elektron sayıları farklı ise kimyasal özellikleri de farklıdır.
[FONT="]Elmas, grafit, amorf karbon, üç madde de yapısında yalnızca karbon (C) u içerir. Fakat uzaydaki dizilişleri ve bağların sağlamlığı farklı olan maddelerdir.[/FONT]
[FONT="]O2 gazı ve O3 (Ozon) gazı birbirlerinin allotropudur. Allotrop için bilinmesi gereken en önemli özellik ise;[/FONT]
[FONT="]Allotrop maddeler bir başka madde ile reaksiyona girdiklerinde aynı cins ürünler oluşur.[/FONT]
[FONT="]2Ca + O2 ® 2CaO[/FONT]
[FONT="]3Ca + 2/3 O3 ® 2CaO gibi.[/FONT]
[FONT="]Modern Teorisi[/FONT]
- Elektron dalga özelliği göstermektedir.
- Atomdaki elektronun aynı anda yeri ve hızı bilinemez.
- Elektronların bulunma ihtimalinin fazla olduğu küre katmanları vardır ve bu katmanlara orbital denir.
- Elektronlar yörüngelere yerleştirilirken ;
- 2n2 formülüne uyarlar.
(n : yörünge sayısı, 1,2,3 ………. gibi tamsayılar) - Son yörüngede maksimum 8 elektron bulunur.
[FONT="]1. yörünge : 2.12 = 2 elektron[/FONT]
[FONT="]2. yörünge : 2.22 = 8 elektron[/FONT]
[FONT="]3. yörünge : 2.32 = 18 elektron[/FONT]
[FONT="]4. yörünge : 2.42 = 32 elektron alır.[/FONT]
[FONT="]
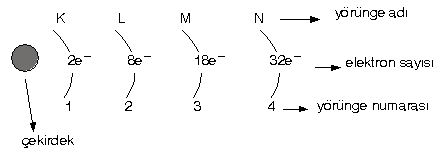
[h=3]Elektronik Konfigürasyon[/h][FONT="]Bir atomun elektronlarının hangi yörüngede olduğu ve orbitallerinin cinsinin belirtildiği yazma düzenine Elektronik konfigürasyon denir.[/FONT]
[FONT="]n : Baş kuant sayısı olup 1, 2, 3, … gibi tam sayılardır. Elektronun hangi yörüngede olduğunu belirtir.
[/FONT]
[FONT="]l : Yan kuant sayısı olup, orbital adı olarak bilinir, s, p, d, f gibi harflerle anılır.[/FONT]
[FONT="]Elektronlar önce düşük potansiyel enerjili orbitallere yerleşirler. Dört değişik enerji düzeyi vardır.[/FONT]
[FONT="]s : Enerji seviyesi en düşük orbitaldir. 2 elektron alabilir.[/FONT]
[FONT="]p : s orbitalinden sonra elektronlar p orbitallerine yerleşir. px , py , pz olmak üzere 3 tanedir. p orbitalleri toplam 6 elektron alabilir.[/FONT]
[FONT="]d : 10 elektron alır ve toplam 5 tanedir. p orbitallerinden sonra elektronlar d orbitallerine yerleşirler.[/FONT]
[FONT="]f : f orbitalleri toplam 14 elektron alır ve 7 tanedir. Enerji düzeyi en yüksek olan orbitaldır.[/FONT]
| Yörünge Sayısı (n) | Yörüngedeki orbital sayısı(n2) | Yörüngedeki elektron sayısı (2n2) |
| 1………. | 1 (1 tane s) | 2 |
| 2. ……… | 4 (1 tane s, 3 tane p) | 8 |
| 3. ……… | 9 (1 tane s, 3 tane p, 5 tane d) | 18 |
| 4. ……… | 16 (1 tane s,3 tane p, 5 tane d, 7 tane f) | 32 |

[FONT="]Bir atomun elektronları yörüngelere yerleştirilirken okların sırası takip edilir. Bunlar bu sıra ile yazılırsa aşağıdaki gibi olur.[/FONT]
[FONT="]1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6[/FONT]
[FONT="]

[FONT="]Periyot : Dizilişi yapılan elementin en son yazılan s orbitalinin başındaki sayıya periyot denir.[/FONT]
[FONT="]Grup : Son yörünge orbitalleri s ve p ile bitiyorsa A grubu, d ve f ile bitiyorsa B grubu elementidir.[/FONT]
- A grupları son yörüngelerindeki s ve p orbitallerindeki elektronların toplamıyla bulunur.